化学部分(70分)
可能用到的相对原子质量:H:l C:12 O:16 Na:23 Cl:35.5
一、选择(本包括10小題,每小题2分,共20分。每小题只有一个选项符合題意)
1.分类是学羽化学的重要方法。下列物质属于氧化物的是
A.O2 B. H2 O C. KCl D.H2SO4
2.膳食中营养搭配有利于人体。下列食品含维生素相对较多的是

A.奶油蛋糕 B.碱面馒头 C.凉拌黄瓜 D.清蒸鲈鱼
3.党的十九大提出要加快生态文明体制改草,速设美丽中国。下列做法正确的是
A.为保护环境,把废旧电油深埋处理
B.为增加粮食产量,大量使用农药、化肥
C.为节约水资,用工业废水直接灌溉农田
D,为节约资源,大力开发新能源替代化石然料
4.下列生用品使用的材料属于有机合成材料的是
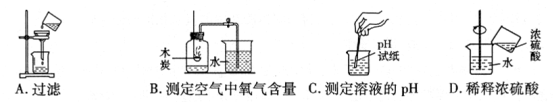
 5.化学实验操作的规范性、安全性是实验成败的关継,同时也反映了实验者的化学素养。下列如图所示的实验操作正确的是
5.化学实验操作的规范性、安全性是实验成败的关継,同时也反映了实验者的化学素养。下列如图所示的实验操作正确的是
 6.元素观、做粒观是化学的重要观念。下列有关元素和做粒的说法不正确的是
6.元素观、做粒观是化学的重要观念。下列有关元素和做粒的说法不正确的是
A.分子、原子和离子都是成物质的粒子
B.同种元素的原子核内质子数与中子数一定相等
C.元素的原子序数与该元素原子核电荷数在数值上相同
D.在物质发生化学变化时,原子的种类不变,元索的种类也不会改变
7,2017年春季,在张献忠沉银现场,考古安家发现了金币、银币、铜币和银锭,还有铁刀、铁矛等兵器,金币银示光亮如初,铁刀铁矛铸迹斑赶。下列说法不正确的是
A,金银铜铁都是重要的金属资源
B.金银的化学性质比铜铁更稳定
C.自然界中,金、银、铜、铁主要以単质的形式存在
D.可以用银、铁、硫酸铜溶液验证银、铁、铜三种金属的活动性顺序
8.下列列化学方程式书写正确的是
A.2H2+O2=2H2O B. 2NaOH+H2SO4=Na2 SO4+H2O
C.2Fe+6HCl=2FeCl3 +3H2 ↑ D.2KMnO4△K2MnO4 +MnO2+O2↑
9.甲、乙两种固体物质的溶解度曲线如右图所示。下列说法不正确的是
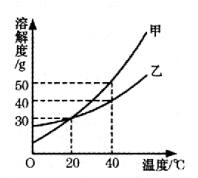
A.40℃时,甲的溶解度大于乙的溶解度
B.甲乙物质的溶解度都随温度的升高面增大
C.20℃时,甲乙溶液中溶质的质量分数一定相等
D.将40℃时乙的饱和溶液降温至20℃,仍然是饱和溶液
10.下列除去物质中所含杂质(捂号内的物质)的方法不正确的是
A | CO2(HCl):通过NaOH溶液后用浓硫酸干燥 |
B | N2(O2):将气体缓缓通过灼热的铜网 |
C | MnO2(KC1):加足量水溶解,过滤,洗涤,干燥 |
D | KNO3溶液(KCI):加适量的AgNO3溶液,过滤 |
二、填空与简答题(本题包括4小题,共22分)
11,(3分)俄罗斯方块你玩过吗?下面是为你设计的化学俄罗斯方块,请根据示例写出下列“口"中对应的化学符号或符号所表达的含义。

12.(6分)(1)化学与我们的生产、生活息息相关。现有干冰、熟石灰、钛合金三种物质,请选择适当的物质填空。
①可用于人工降雨的是 ;
②可用于制造人造骨的是 ;
③可用于改良酸性土境的是 ;
(2)天然气是当今人类使用较多的一种化石燃料,其完全燃烧的化学方程式为 。目前化石燃料日趋枯竭,人类正在积极开发新能源,请你列举一种新能源 :
13.(4分)生活中处处有化学。请按要求回答下列问题。
(1)自来水厂对天然水净化处理得到自来水的过程中,下列操作:①过滤②吸附③消毒④蒸馏,其中没有用到的是 (填序号)。
(2)用自来水烧水的水壶底部,容易形成水垢,水垢的主要成分是碳酸钙和氢氧化镁,可以用厨房中的一种调味品来潸除,这种调味品是 ;
(3)为防止人体缺碘,市售食盐中添加了少量的碘酸钾(KIO3),并在使用说明中强调“不
宜高温烹煮”。碘酸钾与氯酸钾化学性质相似,请写出碘酸钾在加热条件下分解的化学方程式
14.(9分)A、B、C、D、E是九年级化学中常见的五种物质。已知C是人体胃液中可以帮助清化的物质,D是大理石的主要成分,其相互反应及转化关系如下图所示,“一“表示示相连的两物质之间能发生反应,“→”表示一种物质能转化为另一种物质,部分反应条件、反应物、生成物已略去。

(1)写出下列反应的化学方程式。
C与D的反应: ;
B转化为A的反应:
C转化为A的反应: 该反应属于 反应(填基本反应类型)。
(2)B与E的反应是 (填“吸热”或“放热”)反应。
(3)写出E物质的一种用途
三、实验与探究题(本题包括2小题,共20分)
15.(13分)结合下列化学实验装置,回答有关问题。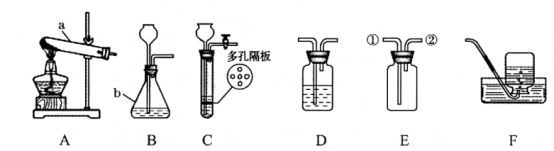 (1)写出图中标有宇母的仪器的名称:a
(1)写出图中标有宇母的仪器的名称:a
2)实验室用氯酸钾制取氧气应选择的发生装置是 (填代号),可用 法收集氧气。制得的氧气用来做如右下图所示的实验,发现H中铁丝不燃烧,其原因是 。写出G中反应的化学方程式
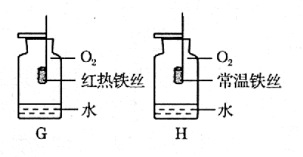
(3)实验室制取二氧化碳常用的药品是 ,若用装置E收集二氧化磯,则 气体应从填“①”或“②")端进入;若要获得干燥的二氧化,可将装置B和装置D用胶皮管连接,并在装置D中盛放 (填物质名称}试剂。
(4)实验室常用装置C代替装置B制取气体,装置C的优点是
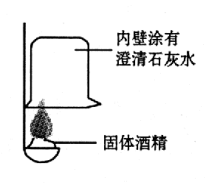
16.(7分)火锅是我国独创的美食,历史悠久。火锅常用的一种燃料是固体酒精。某化学兴趣小组的同学对“固体酒精”产生了好奇,对其成分进行探究。请你回答下列问题。
查阅资料
a.固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比泥合制成。
b.氯化钙、氯化溶液均呈中性。
【提出问题】
①酒精中是否含有碳元素?
②固体酒精中的氢氧化钠是否变质?
【实验探究】
①按右图所示进行实验,发现烧杯内壁有一层白膜,可得出酒精精中含有碳元素的结论,理由是 。
②取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀,请用化学方程式表示该沉淀是如何形成的: 由此说明氢氧化钠已变质。
③为进一步确定氢氧化钠的变质程度,分组进行探究。
甲组同学取烧杯上层清液于两支试管中,按下图所示进行实验。
实验方案 |
|
|
实验现象 | 溶液变红 | 产生 |
实验结论 | 清液中有氢氧化钠 | 清液中有碳酸钠 |
乙组同学认为甲组实验不能证明清液中一定有氢氧化钠,理由是
他们另取烧杯中上层清液,加足量氯化钡溶液,充分反应后,静置,取上层清液,滴加酚酞溶液,酚酞溶液变红。
【反思交流】乙组实验中加足量氯化钡溶液的目的是
【实验结论]小组同学经过讨论,一致认为该固体酒精中的氢氧化钠部分变质。
四、计算题(本题包括2小题,共8分)
17.(2分)断血流滴丸主含有木犀草素(化学式为C13H2Ox,)等黄酮类活性成分,具有止血、抗菌、抗炎及免疫等药理活性。已知木犀草素的相対分子质量为286,请计算
(1)x的值为
2)木犀草素中碳元素的质量分数为 (结果精确到0.1%)
18.(6分)用溶质质量分数为5%的NaOH溶液中和73g的稀盐酸,反应过程中溶液的酸破度变化如下图所示。请计算
(1)用质量分数为10%的氢氧化钠溶液配制5%的氢氧化钠溶液100g,需要水 克.
(2)当a为80g时,所得溶液中溶质的质量分数是多少(结果精确到0.1%)?

参考答案:
化学部分(70分)
一、选择题(本题包括10小题,每小题2分,共20分)
1.B 2.C 3.D 4.A 5.D 6.B 7.C 8.D 9.C 10.A
二、填空与简答题(本题包括4小题,共22分,方程式2分,其余每空1分)
11.(3分)
(1)2NH4+ (2)3SO2 (3)Cl2
12.(6分)
(1)①干冰 ②钛合金 ③熟石灰
(2)①CH4+2O2 2H2O+ CO2 太阳能(其他合理答案也可)
13.(4分)(1)④ (2)醋 (3)2KIO3 △ 2KI +3O2 ↑
14.(9分)
(1)CaCO3+2HCl=CaCl2+H2O+CO2 ↑ 2H2O![]() 2H2↑+O2 ↑
2H2↑+O2 ↑
Zn+2HCl= ZnCl2+H2 ↑(其他合理答案也可) 置换
(2)放热
(3)作食品干燥剂(其他合理答案也可)
三、实验与探究题(本题包括2小题,共20分)
15.(13分)
(1)试管(1分) 锥形瓶(1分)
(2)A(1分) 排水(或向上排空气)(1分)
H中铁丝的温度未达到着火点(1分) 3Fe+2O2![]() Fe3O4(2分)
Fe3O4(2分)
(3)大理石(或石灰石)与稀盐酸(2分) ①(1分) 浓硫酸(1分)
(4)可以随时控制反应的发生与停止(2分)
16.(7分)
烧杯内壁出现白膜说明有CO2生成,依据化学反应前后,元素的种类不变,所以酒精中含有碳元素(2分) Na2CO3+CaCl2=CaCO3↓+2NaCl(2分) 白色沉淀(1分)
碳酸钠溶液也能使酚酞溶液变红(1分) 除去碳酸钠,以免对氢氧化钠的检验造成干扰(1分)
四、计算题(本题包括2小题,共8分)
17.(2分)(1)6(1分) (2)62.9% (1分)
18.(6分)(1)50(2分)
(2)设生成氯化钠的质量为x
NaOH + HCl=NaCl+H2O
40 58.5
80g×5% x(1分)
40: 80×5%=58.5:x x=5.85g(1分)
反应后所得溶液中溶质的质量分数为![]() ×100%=3.8% (2分)
×100%=3.8% (2分)

孔乙己是贫困潦倒的知识分子。在书中,孔乙己是一个知识分子,满口“之乎者也”,但是他很穷,还窃书,说过“读书人的事,怎么能叫窃,”被人嘲笑,他...

自然界产生氧气的化学方程式:光合作用的反应式为6CO2+12H2O→C6H12O6+6O2+6H2O。包括光反应和暗反应两个过程。需要具备光...

有的高校没有条件,只要学业水平成绩都合格就可以,比如中国科学院大学。有的需要平常学习考试成绩,比如北京外国语大学要求高三第一学期期末成绩在全...

在四则运算中,表示计算顺序,在小括号之后、大括号之前;表示两个整数的最小公倍数;表示取未知数的整数部分;在函数中,表示函数的闭区间;在线性代...

济南开设的最好的职高学校有:济南方信集团职业高中、济南公共交通职业高中。济南市公共交通职业高级中学是由济南市公共交通总公司承办,业务属济南市...

实然:是说事物实际上就是这样的,但不同于现实性(现实性指其有合理性和客观性);应然:就是应该是怎么样的意思,比如说这件事,就应该是那样的结果...

地中海气候一种夏季炎热干燥、冬季温和多雨,雨热不同期的气候类型。地中海气候冬季受西风带控制,锋面气旋频繁活动,气候温和,最冷月的气温在4-1...

碱石灰,又称钠石灰,碱石灰是白色或米黄色粉末,疏松多孔,是氧化钙(CaO,大约75%),水(H₂O,大约20%),氢氧化钠(NaOH,大约3...